Rufen Sie uns einfach an, und wir beraten Sie gerne zu unserem Seminar- und Studienangebot.
Unsere Ansprechpartner:

Michael Rabbat, Dipl.-Kfm.
MBA Chief Operating Officer

Claudia Hardmeier
Kunden-Center
Studienbetreuung
2.4. Gegenüberstellung, Vorgaben für Zulassungen von Medizinprodukten in der EU vs. Schweiz
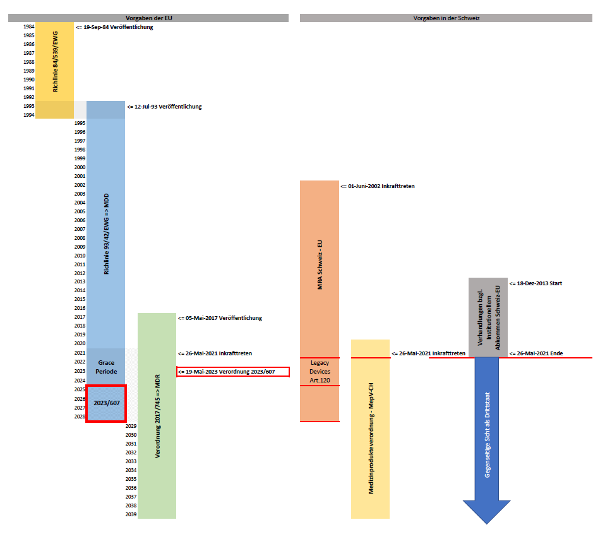
Abbildung 1 (Gegenüberstellung Vorgaben EU vs. CH)
Wie aus den Darstellungen (Abbildung 1) zur Historischen Entwicklung der Vorgaben zur Zulassung von Medizinprodukten in der EU und der Schweiz zu erkennen ist, waren diese bis zum Inkrafttreten der MDR und unter Berücksichtigung des MRA weitgehendst harmonisiert. Der Abbruch der Verhandlungen zum Institutionellen Abkommens (InstA) mit direktem Einfluss auf das MRA führt zu tiefgreifenden Herausforderungen für den Schweizer Medizinproduktemarkt.
Herausforderungen bestehen besonders in nachfolgenden Sektoren, bzw. deren beteiligten:
- Herausforderungen für Europäische Medizinproduktehersteller zum Schweizer Markteintritt
- Herausforderungen für Schweizer Medizinproduktehersteller zum Europäischen Markteintritt
- Versorgungsengpass von Schweizer Patienten durch erschwerte Einfuhr/Anerkennung von Medizinprodukten.







