Rufen Sie uns einfach an, und wir beraten Sie gerne zu unserem Seminar- und Studienangebot.
Unsere Ansprechpartner:

Michael Rabbat, Dipl.-Kfm.
MBA Chief Operating Officer

Claudia Hardmeier
Kunden-Center
Studienbetreuung
3.4. Versorgungssicherheit mit Medizinprodukten für Schweizer Gesundheitseinrichtungen
Wie aus dem Branchenbericht der SMTI 2022 abzuleiten ist, besteht für den Schweizer Gesundheitsmarkt eine potenzielle Versorgungsunsicherheit mit ausländischen Medizinprodukten.
Dies ist wie folgt abzuleiten.
Seit 26. Mai 2021 ist die MDR und die MepV gültig. Vor allem Klasse I Produkte müssen seitdem die Anforderungen der MDR/MepV erfüllen[1] (nicht Klasse 1s, 1r, 1m – siehe Abschnitt MDR). Rund 40% der Schweizer Hersteller (siehe Abbildung 10) geben bei der SMTI-Umfrage an, dass sie ihr Produktportfolio reduzieren werden. Rund 82% der in der Schweiz ansässigen Händler rechnen mit einer Produktportfolio Reduktion. Durchschnittlich ist mit einer Produktportfolio Reduktion von 7% (bei Herstellern) und 15% bei Händlern zu rechnen.
- Die unterschiedliche Beurteilung von Herstellern und Händlern lässt sich mit der Größe der Absatzmärkte erklären. Während Schweizer Hersteller den Zusatzaufwand angesichts des großen EU-Marktes leisten, sind Händler auf Produkte von ausländischen Herstellern angewiesen. Diese sind aufgrund der erhöhten Anforderungen (z.B. Benennung CH-REP) des Öfteren nicht bereit, den kleinen Schweizer Markt weiterhin zu bedienen.
- Spitaler bestätigen, dass Produkte ausländischer Hersteller fehlen. Sie bekunden Schwierigkeiten bei der Beschaffung von Ersatzprodukten (SMTI: helbling, 2022)

Abbildung 12 Quelle SMTI-Umfrageergebnis 2022 (swiss medtech & helbling)
Zwar wurde ausländischen Herstellern mit der vom Schweizer Bundesrat vorgenommenen Änderung der MepV bzw. mit dem Erlass der Übergangsfristen zusätzliche Zeit für die Benennung eines CH-REP eingeräumt, damit wird die Gefahr der eintretenden Versorgungsengpässe jedoch nicht mehr gebannt. Vielmehr ist zu erwarten, dass sich die meisten Versorgungsengpässe nach Ablauf dieser zu kurzen Übergangsfristen manifestieren werden. Offen ist hier vor allem die Frage, wie Schweizer Gesundheitsakteure an Substitutionsprodukte gelangen sollen, wenn die Mehrheit der Hersteller aus den EU-Staaten keinen CH-REP benennt. Da die Schweiz nicht in der Lage ist, diese große Anzahl und Vielfalt an Medizinprodukten selbst herzustellen, müsste diesfalls der Bezug von Ersatzprodukten zwangsweise außerhalb des EU-Raums erfolgen. Dabei stellt sich jedoch das Problem, dass solche Medizinprodukte aus Drittstaaten, welche anderen Regulierungssystemen unterliegen, heute nicht regulär in die Schweiz importiert werden dürfen und diese nach heutigem Recht ebenfalls einen CH-REP benötigen würden.
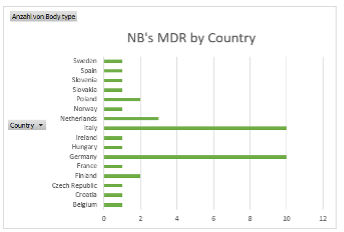
Abbildung 13 Anzahl NB's unter MDR; Grafik Dietmar Holzhammer; Quelle: (Commission, 2023)
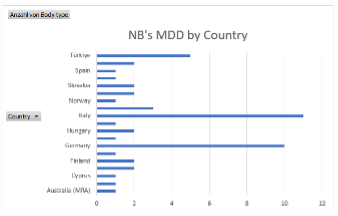
Abbildung 14 Anzahl NB's unter MDD; Grafik Dietmar Holzhammer; Quelle: (Commission, 2023)

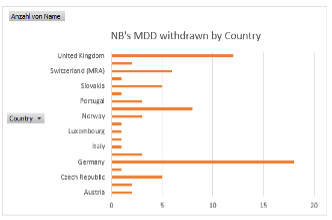
Abbildung 15 Anzahl ehemaliger NB's unter MDD; Grafik Dietmar Holzhammer; Quelle: (Commission, 2023)
[1] Johner Institut: Merkblatt-MDR-Uebergangsfristen-V18







