Rufen Sie uns einfach an, und wir beraten Sie gerne zu unserem Seminar- und Studienangebot.
Unsere Ansprechpartner:

Michael Rabbat, Dipl.-Kfm.
MBA Chief Operating Officer

Claudia Hardmeier
Kunden-Center
Studienbetreuung
3. Herausforderungen und Ableitungen aus der Branchenanalyse
3.1. Herausforderungen für Europäische Medizinproduktehersteller zum Schweizer Markteintritt
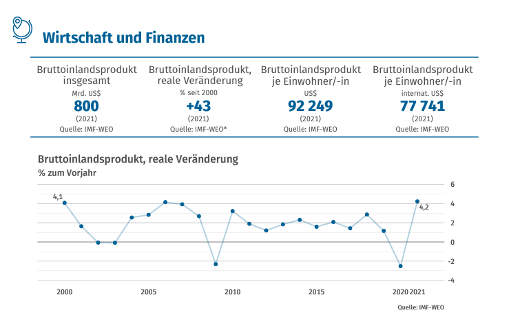
[1] Vgl. Swiss medtech – medica.device.forum vom 12. Mai 2022
[1] Vgl. Handelsstatistik zum Abkommen der Schweiz und der EU (MRA)-2021 SECO

Abbildung 3 SMTI Branchenstudie 2022 (swiss medtech & helbling)
Aufgrund des gescheiterten Institutionellen Abkommens (InstA) und dem daraus resultierend nicht mehr gültigen Mutual Recognition Agreements (MRA) wird die Schweiz nun aus Sicht eines Medizinprodukteherstellers aus der EU als Drittstaat betrachtet. Ungeachtet der Anforderung der Schweiz durch die Medizinprodukte Verordnung (MepV), welche grundlegend auf der Medizinprodukteverordnung (EU) 2017/745 (MDR) aufbaut und somit eine CE-Kennzeichnung voraussetzt muss ein Hersteller mit seinem Sitz außerhalb der Schweiz einen Schweizer Bevollmächtigten (CH-REP) nachweisen.
Die Swissmedic hat in Ihrem Merkblatt zu Pflichten von Wirtschaftsakteuren[1] eine detaillierte Beschreibung zu Pflichten und Übergangsbestimmungen für Wirtschaftsakteure mit Sitz in der Schweiz und für Produkte, welche in der Schweiz auf dem Markt bereitgestellt werden, herausgegeben.
Die folgende Abbildung und die dazugehörigen Legenden erklären anhand eines Beispiels eines nicht in der Schweiz ansässigen Herstellers die Lieferkette innerhalb der Schweiz und die Rollen der Wirtschaftsakteure.
Andere Konfigurationen (z.B. CH-REP = Importeur und Händler oder ohne Händler) sind auch möglich.

[1] Swissmedic VM-ID: MU600_00_016d / V4.0 / mea / pmi / 06.04.2023
 |
Produkt(e) (Art. 1 Abs. 1 MepV)
Beinhaltet Medizinprodukte und deren Zubehör, sowie Produkte ohne medizinische Zweckbestimmung. Hinweis: der Begriff Medizinprodukt umfasst auch In-vitro-Diagnostika und deren Zubehör. |
 |
Hersteller (Art. 4 Abs. 1 Bst. f MepV, Art. 4 Abs. 1 Bst. e IvDV)
Natürliche oder juristische Person, die ein Produkt herstellt oder neu aufbereitet beziehungsweise entwickeln, herstellen oder neu aufbereiten lässt und dieses Produkt unter ihrem eigenen Namen oder ihrer eigenen Marke vermarktet. Die Pflichten des Herstellers gelten auch für Personen, welche die Tätigkeiten gemäß Art. 16 Abs. 1 MDR bzw. Art. 16 Abs. 1 IVDR vornehmen; Art. 4 Abs. 1 Bst. f MepV / Art. 4 Abs. 1 Bst. e IvDV. |
| Bevollmächtigter in CH (Art. 4 Abs. 1 Bst. g MepV, Art. 4 Abs. 1 Bst. f IvDV)
Natürliche oder juristische Person in der Schweiz, die von einem im Ausland ansässigen Hersteller schriftlich beauftragt (Mandat) wird, in seinem Namen bestimmte Aufgaben gemäß MepV / IvDV wahrzunehmen. Hat der Hersteller eines Produktes seinen Sitz nicht in der Schweiz, so dürfen seine Produkte nur in Verkehr gebracht werden, nachdem ein Bevollmächtigter mit Sitz in der Schweiz mandatiert, wurde. Dies gilt auch für Hersteller mit Sitz in der EU/EWR. Die Benennung des Bevollmächtigten gilt mindestens für alle Produkte einer generischen Produktgruppe. |
|
 |
Importeur (Art. 4 Abs. 1 Bst. h Mep, Art. 4 Abs. 1 Bst. g IvDV)
Ein Importeur wird nicht «benannt», sondern die Rolle ergibt sich aus der Tätigkeit, welche ausgeübt wird, wenn eine natürliche oder juristische Person in der Schweiz ein Produkt aus dem Ausland auf dem Schweizer Markt in Verkehr bringt. |
 |
Händler (Art. 4 Abs. 1 Bst. i MepV, Art. 4 Abs. 1 Bst. h IvDV)
Wirtschaftsakteur in der Lieferkette, der ein Produkt bis zum Zeitpunkt der Inbetriebnahme auf dem Schweizer Markt bereitstellt, mit Ausnahme des Herstellers oder des Importeurs. |
| Bereitstellung auf dem Markt (Art. 4 Abs. 1 Bst. a MepV, Art. 4 Abs. 1 Bst. a IvDV)
Sammelbegriff, bezeichnet die Übertragung oder Überlassung eines Produkts. Das Anwenden eines Produktes durch eine Fachperson (z.B. eines Implantates oder von Verbandmaterial) ist kein Bereitstellen auf dem Markt. Die Bereitstellung eines Produkts setzt ein Angebot oder eine (schriftliche oder mündliche) Vereinbarung zwischen zwei oder mehr juristischen oder natürlichen Personen in Bezug auf die Übertragung des Eigentums, des Besitzes oder sonstiger Rechte hinsichtlich des betreffenden Produkts nach dessen Herstellung voraus, was nicht zwingend die physische Übergabe des Produkts erfordert. Diese Übertragung kann entgeltlich oder unentgeltlich erfolgen. |
|
 |
Inverkehrbringen (Art. 4 Abs. 1 Bst. b MepV, Art. 4 Abs. 1 Bst. b IvDV)
Erstmalige Bereitstellung eines Produkts auf dem Schweizer Markt (z.B. durch Übertragung oder Überlassung zwischen Wirtschaftsakteuren oder von einem Schweizer Wirtschaftsakteur zu einer Gesundheitseinrichtung / zur Verbraucherin). Der Begriff des Inverkehrbringens bezieht sich auf jedes einzelne Produkt, und nicht auf eine Produktart. Daher wird jedes einzelne Produkt in Verkehr gebracht, auch wenn Produkte derselben Art (oder Modell oder Typ) bereits vorher in Verkehr gebracht wurden. |
 |
Inbetriebnahme (Art. 4 Abs. 1 Bst. c MepV, Art. 4 Abs. 1 Bst. c IvDV)
Zeitpunkt, zu dem das Produkt erstmals den Endanwenderinnen bzw. Gesundheitseinrichtungen zur Verfügung gestellt wird. |
 |
Gesundheitseinrichtung (Art. 4 Abs. 1 Bst. k und l MepV, Art. 4 Abs. 1 Bst. j IvDV) |
Abbildung 5 Legende Inverkehrbringen von Produkten & Wirtschaftsakteuren (Quelle 5-Swissmedic)
Wie aus Abbildung 4, Abbildung 5 und der Branchenanalyse zu entnehmen ist, lassen sich die wesentlichen neuen Herausforderungen für Europäische Medizinproduktehersteller, um Produkte auf dem Schweizer Markt zur Verfügung zu stellen, wie folgt zusammenfassen.
- Benennung eines Bevollmächtigten in der Schweiz[1]
- Hierzu sind entsprechende vertragliche Regelungen zur gegenseitigen Absicherung und Klarstellung der Regulatorischen Verantwortlichkeiten zu treffen
- Weiterhin sind in diesem Zuge auch die unterschiedlichen Verantwortlichkeiten zwischen Bevollmächtigten, Importeur und Händler eindeutig abzugrenzen[2].
- Business Case vor allem für Klasse I & „nischen-Produkte“ mit geringen Stückzahlen und geringer Marge. Frage: „Ist der Schweizer Markt nach all diesen zusätzlichen Anforderungen/Kosten für den Hersteller weiterhin interessant?“
[1] Gilt nicht für Lichtenstein, aufgrund eines bestehenden Zollvertrages zw. CH & Lichtenstein
[2] Swissmedic, Kapitel 5 / Pflichten VM-ID: MU600_00_016d / V4.0 / mea / pmi / 06.04.2023







