Rufen Sie uns einfach an, und wir beraten Sie gerne zu unserem Seminar- und Studienangebot.
Unsere Ansprechpartner:

Michael Rabbat, Dipl.-Kfm.
MBA Chief Operating Officer

Claudia Hardmeier
Kunden-Center
Studienbetreuung
2.4.2.6. DIN ISO 9000- Normfamilie
Mit EN ISO 9000 ff. werden Anforderungen an Qualitätsmanagementsysteme beschrieben.
Die Anforderungen sin allgemein formuliert, so dass die Anwendung in Unternehmen aller Branchen sichergestellt werden kann.228
Ebenso wie beim Total Quality Management handelt es sich bei ISO 9000- Normen um Qualitätsmanagement in einem sehr umfassenden Sinn. um Diese Norm basiert auf Grundsätzen der Kundenorientierung, Prozessorientierung und kontinuierlicher Verbesserung.229 Ebenso werden ein starker Miteinbezug der Mitarbeiter, der systemorientierte Ansatz, eine sachbezogene Entscheidungsfindung sowie Lieferantenbeziehungen betont.230 Die Norm besagt welche Richtlinien befolgt werden sollen, aber zur Beantwortung der Frage wie diese umzusetzen sind, sind branchenabhängig weitere Vorgaben notwendig. Für die Prozessorientierung wird das Geschäftsprozessmanagement benötigt.
In der Pharmabranche sind bezüglich Qualitätsmanagements die Anforderungen nach GMP (Good Manufacturing Practice) einzuhalten. GMP bedeutet «Gute Herstellungspraxis» und ist „in Gesetzen, Verordnungen und Leitfäden weltweit verankert. Diese Anforderungen betreffen Methoden, Anlagen oder Kontrollen, die zur Herstellung, Verarbeitung, Verpackung und /oder Lagerung von Arzneimitteln eingesetzt werden. Sie sollen gewährleisten, dass Arzneimittel die erforderlichen Qualitätsmerkmale erfüllen, indem sie gleichbleibend produziert und geprüft werden entsprechend den Zulassungsunterlagen.231 Während die ISO- Norm auf die Erreichung der Qualität des gesamten Managementsystems unter Berücksichtigung aller Unternehmensbereiche abzielt, dienen die Vorgaben nach GMP der Sicherstellung der Produktqualität während sämtlicher Herstellungs- und Kontrollaktivitäten. Somit ergänzen ISO- Normen bestehende Qualitätsmanagementsysteme in Bereichen, welche bis dato durch GMP- Anforderungen nur begrenzt abgedeckt werden.
In einem Qualitätsmanagementhandbuch werden unternehmensspezifische Grundaspekte zu Leitbild, Aufbauorganisation, Ablauforganisation, Managementverantwortung, Verfahrens- und Prüfanweisungen sowie Massnahmen zur kontinuierlichen Verbesserung des Qualitätsmanagementsystems zusammengefasst.
Durch die enge Beziehung zwischen Qualitätsmanagement und Geschäftsprozessmanagement ist eine Verbindung beider Systeme zu berücksichtigen.232
Demzufolge ist in auf ISO- Norm basierenden Prozessanweisungen an den entsprechenden Stellen auch auf die branchenspezifischen Dokumente, wie Standard Operating Procedures (SOP), zu verweisen, welche auf den GMP- Richtlinien basieren.
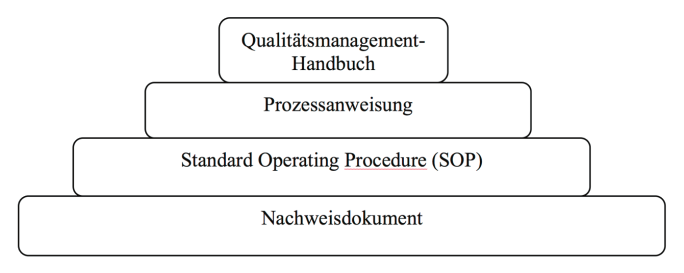
Abb. 10: Hierarchie der Dokumente innerhalb ein eines Qualitätsmanagementsystems (eigene Darstellung)
Zur Vermeidung der Vermischung von Dokumentationsebenen sollte eine Abgrenzbarkeit stets gegeben sein. Ebenso ist auf eine logische und durchgehende Nomenklatur zu achten.
228 Vgl. http://www.swissts.ch/de/zertifizierung-von-unternehmen/produkte/iso-9001/ [30.11.2013]
229 Vgl. Schmelzer/Sesselmann (ISO 9000ff.:2000 und Geschäftsprozessmanagement), S.40
230 Vgl. Allweyer (Qualitätsmanagementsystem nach ISO 9000), S.279
231 Definition «GMP» nach EU- GMP- Leitfaden (Mindestanforderungen für Arzneimittel), Kapitel 3.1, S.9
232 Vgl. Schmelzer/Sesselmann (ISO 9000ff.:2000 und Geschäftsprozessmanagement), S.42







